In Parkinson’s disease, certain nerve cells die in the brain. Patients can only slow down and their muscles become stiff. Arms and legs begin to tremble in peace. Many patients also have problems thinking and become demented. Read here: What is Parkinson exactly? Who is affected? How does he express himself? What treatment options are there?

Parkinson’s: short overview
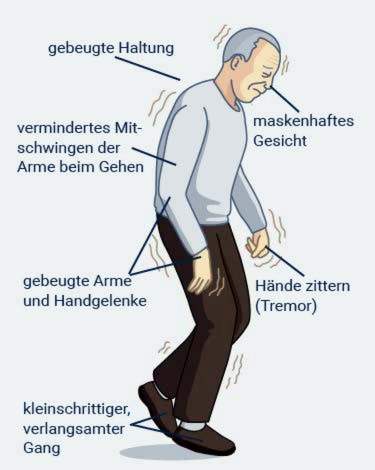
- Typical symptoms: Slow movements, lack of exercise, muscle stiffness, shaking at rest, lack of stability of the upright posture, rigid facial expressions
- Causes:Parkinson’s disease: dying of dopamine-producing cells in the brain; secondary to Parkinson’s disease: other disorders, drugs or intoxications; Genetic Parkinson’s syndrome: genetic changes
- Important investigations: Physical and neurological examination, L-Dopa test, computed tomography (CT), magnetic resonance imaging (MRI)
- Treatment options: Medications (like Levo-Dopa), physiotherapy, speech therapy, occupational therapy, deep brain stimulation (THS)
Parkinson’s: symptoms
Stiff muscles, slowed movements and trembling hands are typical features of Parkinson’s disease.
Parkinson’s early symptoms
Signs of progressive brain disease can occur years before the main symptoms. Such parkinsonian early symptoms are:
- REM Sleep Behavioral Disorder: Normally a person in dream sleep is “paralyzed”. In the REM sleep behavior disorder the dreamy movements are partly carried out (speaking, laughing, gesturing, etc.). This can be dangerous for the person affected and the sleeping partner.
- Sense of smell is reduced or completely absent (hyposmia / anosmia)
- Pain in muscles and joints (dysaesthesia), often in the area of shoulder and arm
- the arms swing less when walking
- Getting up, washing, dressing, eating, etc. take longer than before
- constipation
- Visual disturbances (such as disturbed color vision)
- the handwriting seems cramped and becomes smaller, especially at the end of a line or page
- depressions
- Tiredness, exhaustion
- stiff, uncertain feeling, shakiness
- the patient withdraws and neglects his hobbies
Many of these parkinsonian early symptoms are very nonspecific. So you can also have many other causes (such as the advanced age). Therefore, they are often not recognized as early signs of Parkinson’s.
REM sleep behavior disorder
The most important early sign is the REM sleep behavior disorder: those who show this type of sleep disorder generally have an increased risk of so-called neurodegenerative diseases. These are progressive diseases that accompany the loss of nerve cells. Most people with a REM sleep disorder later develop Parkinson’s disease. Others get sick with a certain form of dementia (Lewy body dementia).
Parkinson’s: main symptoms
The Parkinson’s disease symptoms usually develop slowly. Relatives and friends often catch them earlier than the patient.
Most Parkinson’s symptoms begin one-sided, that is, on only one side of the body. Later, they spread to the other side. In the course of the disease, they are also becoming more pronounced.
The typical Parkinson’s symptoms are:
- slowed movements (bradykinesis) to low-movement (hypokinesis) or immobility (akinesia)
- stiff muscles (rigor)
- Muscle tremors at rest (Parkinson’s tremor)
- lack of stability of upright posture (postural instability)
Slowed movements (bradykinesis): All body movements are unnaturally slow. This means, for example, that people with Parkinson’s disease are noticeably slow and walking in small steps. Over time, the walk shuffles, and patients go forward bent. That’s one of the most obvious symptoms. Parkinson’s patients can also sit down slowly and with difficulty and get up again. Sometimes the affected people are suddenly blocked in their movements – they seem to freeze. This is what medical professionals call “freezing”.
The symptoms of Parkinson’s disease also affect the gestures and facial expressions: the face increasingly acts like a rigid mask. Those affected usually speak quietly and monotonously, so they are harder to understand. Swallowing often causes them problems, such as drinking or eating. Another Parkinson’s symptom is a disturbed fine motor skills: For example, those affected are having a hard time writing something, buttoning their coat or brushing their teeth.
When the body movements are particularly slow or the patient is partially completely motionless, doctors speak of akinesia (akinesia).
Rigid muscles:In Parkinson’s there are no paralysis, but the muscle strength is largely preserved. The muscles are permanently tense, even at rest. This is painful for those affected. Especially the shoulder and neck area can hurt.
The muscle stiffness can be demonstrated by the so-called Cogwheel rigidity: When the doctor tries to move the patient’s arm, it is prevented by the stiff muscles. Therefore, the arm can only move a little bit and jerky. It almost feels like there is a gear in the joint that only allows the movement to the next notch and then clicks into place. The gear phenomenon is usually tested in the elbow or wrist. It is a typical Parkinson’s disease, but it can also occur in other diseases.
Muscle tremors at rest (rest tremor): In Parkinson’s disease, arms and legs typically begin to tremble at rest. Therefore, the disease is also called “shaking palsy”. One side of the body is usually more affected than the other. In addition, the arm usually trembles more than the leg.
Parkinson’s tremor characteristically occurs at rest. This can distinguish Parkinson’s from other disorders with tremor (tremor). If, for example, the hand does not tremble in peace, but as soon as you want to perform a targeted movement, doctors speak of the so-called intentional tremor. Its cause is a damage or disturbance in the cerebellum.
Incidentally, most people who shiver have neither Parkinson’s disease nor any other recognizable neurological disorder. The cause of this “essential tremor” is unknown.
Lack of stability of upright posture: Everybody unconsciously corrects his posture when walking and standing upright at any time. The whole thing is controlled by so-called control and holding reflexes. Reflexes are automatic movements that are triggered by certain stimuli. These are unconscious, involuntary movements or muscle tensions. The holding and adjusting reflexes of the person are responsible for the fact that one can automatically balance the body even during movement and does not fall.
In Parkinson’s disease, the setting and holding reflexes are typically disturbed. Affected individuals therefore struggle to maintain their stability. This is called postural instability. It is the reason why Parkinson’s patients can no longer easily “catch” sudden, unforeseen movements, such as tripping or a sudden gust of wind. Therefore, they are uncertain when walking and fall easily.
Parkinson’s: accompanying symptoms
Main Parkinson’s symptoms are sometimes accompanied by other complaints:
Parkinson’s patients have one more often depression as healthy and as people with other chronic diseases. Sometimes the depression develops only in the course of Parkinson’s disease. In other patients, it precedes the motor symptoms (slowing down movement, etc.).
In addition, in Parkinson’sdecrease intellectual capacity and a dementia arise (see below). Those affected are increasingly having difficulty thinking. However, one should not forget that even the most healthy people can think slower and remember things harder as they get older. So that does not necessarily have to be a sign of Parkinson’s.
In many Parkinson’s patients facial skin produces excess sebum. It looks greasy and shiny. Doctors speak of so-called “Ointment face”: The patient’s face looks as if the person had applied a thick layer of ointment or face cream.
Parkinson’s symptoms also include bladder disorders: many patients are unable to properly control their bladder. So it can happen that involuntary urination (incontinence) and the patients themselves wet at night (Enuresis). But the opposite is also possible: Some patients have problems leaving water (urinary retention).
The intestine is often sluggish in Parkinson’s, so get a constipation developed. Such constipation can also occur as an early sign of Parkinson’s.
Sometimes men show up potency problems (Erectile dysfunction). This impotence can be caused by both the disease itself and Parkinson’s drugs.
All the accompanying symptoms can also be triggered by other diseases, not just Parkinson’s.
Parkinson’s disease
Parkinson’s patients are more susceptible to dementia than the general population: About one third of patients also develop dementia during the course of the disease. According to some studies, the risk of Parkinson’s dementia is even higher (up to 80 percent).
The symptoms of Parkinson’s dementia include primarily one disturbed attention and a slowed thinking, That’s an important difference to Alzheimer’s – the most common form of dementia. Alzheimer’s patients mainly suffer from memory disorders. In contrast, Parkinson’s dementia does not occur until later stages of the disease.
Read more in the article Dementia in Parkinson’s.
Parkinson’s: causes
Physicians also diagnose Parkinson’s disease Primary or idiopathic Parkinson’s disease (IPS), “Idiopathic” means that no tangible cause for the disease can be found. This “real” Parkinson’s makes up about 75 percent of Parkinson’s syndromes. He is in the focus of this text. To distinguish from these are the rare ones genetic forms of Parkinson’s disease, the “secondary Parkinson’s syndrome” and the “Atypical Parkinson’s syndromeThey will be briefly described below.
Idiopathic Parkinson’s: dopamine deficiency
Parkinson’s disease is caused by a specific brain region, the so-called “black substance” (substantia nigra) in the midbrain. This brain region contains a lot of iron and the dye melanin. Both colors the “Substantia nigra” strikingly dark (in comparison to the otherwise bright brain tissue).
In the “Substantia nigra” are special nerve cells that produce the neurotransmitter dopamine. Dopamine is very important for controlling movements. In idiopathic Parkinson’s, more and more dopamine-producing neurons die. Why, you do not know.
Due to this progressive cell death, the level of dopamine in the brain continues to decrease – it develops dopamine deficiency, The body can balance it for a long time: Only when about 60 percent of the dopamine-producing nerve cells have died, is the dopamine deficiency noticeable: the patient is moving more and more slowly (bradykinesis) or partially no longer (akinesia).
But the dopamine deficiency itself is not the sole cause of Parkinson’s disease: it also brings the sensitive Balance of neurotransmitters out of balance: Because less and less dopamine is present, for example, the amount of the messenger acetylcholine increases in relative terms. Experts suggest that this is the cause of tremor and rigidity in Parkinson’s disease.
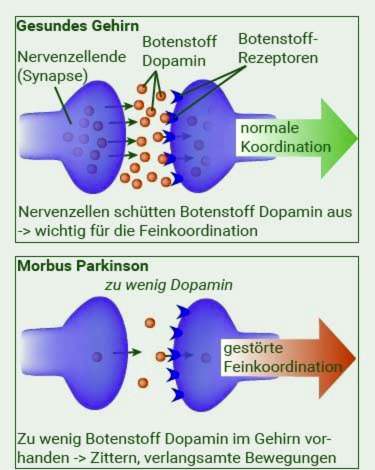
The imbalance of neurotransmitters in Parkinson’s could also be responsible for the fact that many patients become additionally depressed. Because one knows that generally with depression the balance of the neurotransmitters is disturbed. The connection between Parkinson’s disease and depression has not yet been conclusively resolved.
Parkinson’s Causes: Many assumptions, few evidence
Why in Parkinson’s disease nerve cells in the “substantia nigra” die, is still unclear. Research suggests that several factors are involved in the development of Parkinson’s disease.
For example, scientists have found that nerve cells in Parkinson’s patients can only adequately remove harmful substances. Cell-damaging substances are, for example, the so-called “free radicals”. These are aggressive oxygen compounds that arise in various metabolic processes in the cell.
Parkinsonian nerve cells may not be able to break down these dangerous substances before they cause harm. Or the detoxification ability of the cells is normal, but it produces an excessive amount of “free radicals” in Parkinson’s. In both cases, the cell-damaging substances in nerve cells could accumulate and kill them.
There are other possible Parkinson’s causes that are currently being discussed and researched.
Genetic forms of Parkinson’s
If a family member is suffering from Parkinson’s disease, this unsettles many relatives. You wonder if Parkinson’s is inheritable. In the vast majority of cases, however, Parkinson’s is the idiopathic Parkinson’s disease described above. Inheritance is not an issue in this sporadic disease form, experts believe.
This is different in the so-called monogenetic forms of Parkinson’s: each of them is caused by the mutation in a particular gene. These gene mutations can be passed on to the offspring. Monogenic forms of Parkinson’s are inheritable. They are also often called familial Parkinson’s syndrome designated. Luckily, they are rare.
Secondary Parkinson’s syndrome
In contrast to idiopathic Parkinson’s, symptomatic (or secondary) Parkinson’s syndrome has clearly identifiable causes. These include:
- Medicines: Dopamine inhibitors (dopamine antagonists) such as neuroleptics (for the treatment of psychosis) or metoclopramide (for nausea and vomiting), lithium (for depression), valproic acid (for seizures), calcium antagonists (for high blood pressure)
- other diseases such as brain tumors, inflammation of the brain (eg due to AIDS), hypofunction of the parathyroid glands (hypoparathyroidism) or Wilson’s disease (copper storage disease)
- Poisoning, with manganese or carbon monoxide
- Injuries of the brain
Atypical Parkinson’s syndrome
Atypical Parkinson’s syndrome develops as part of various neurodegenerative diseases. These are diseases in which neurons progressively die off in the brain. In contrast to idiopathic Parkinson’s syndrome, this cell death affects not only the “substantia nigra”, but also other brain regions. Therefore, atypical Parkinson’s syndrome in addition to Parkinson-like symptoms even more symptoms.
Neurodegenerative diseases that can cause atypical Parkinson’s syndrome include:
- Lewy body dementia
- Multisystem atrophy (MSA)
- Progressive supranuclear palsy (PSP)
- Corticobasal degeneration
Such diseases have a significantly worse prognosis than the “real” (idiopathic) Parkinson’s syndrome.
Incidentally, the drug “L-Dopa”, which works very well in idiopathic Parkinson’s, hardly or not at all helps with atypical Parkinson’s.
Parkinson’s: treatment
Parkinson’s therapy is individually adapted to each patient. Because the disease symptoms can vary from person to person and progress at different rates.
Mostly Parkinson is with drugs sometimes mild symptoms sometimes do not require therapy at first. Which active ingredients are used depends primarily on the age of the patient. Sometimes a neurosurgical procedure can be useful – the so-called Deep brain stimulation (Deep Brain Stimulation, DBS).
In addition to medical and possibly surgical measures, the individual Parkinson’s treatment may include other building blocks. These include, for example physical therapy, speech therapy and occupational Therapy, It makes sense in any case, to be treated in a special Parkinson’s clinic.
Parkinson’s therapy: medication
There are several medications for Parkinson’s therapy. They help against ailments such as slow movements, stiff muscles and tremors. However, they can not prevent the death of the nerve cells and thus the progression of the disease.
The typical Parkinson’s symptoms are triggered by a lack of dopamine in the brain. Thus, they can be alleviated either by supplying the messenger substance as a drug (for example in the form of L-Dopa) or by stopping the breakdown of the existing dopamine (MAO-B inhibitors, COMT inhibitors). Both mechanisms compensate for dopamine deficiency. They largely eliminate the typical Parkinson’s symptoms.
L-dopa (levodopa)
Parkinson’s patients to administer the missing dopamine directly as a syringe or tablet, has no sense: The messenger is indeed transported through the bloodstream to the brain. But he can not overcome the protective blood-brain barrier, so do not get directly into the nerve tissue. The Precursor of dopamine but is capable of: This L-Dopa (levodopa) is therefore suitable for the treatment of Parkinson’s. When it reaches the brain, it is converted into dopamine by the enzyme Dopa decarboxylase. This can then develop its effect in the brain and alleviate Parkinson’s symptoms such as muscle stiffness (rigor).
L-Dopa is very effectiveand hashardly any side effects, It is usually taken in the form of tablets, capsules or drops. Doctors prescribe it especially in patients over the age of 70. In younger patients L-dopa, however, is used only very restrained. The reason is that the treatment with L-dopa after a few years movement disorders (dyskinesias) and effect fluctuations (effect fluctuations) can trigger (see side effects).
L-dopa is always combined with another active ingredient, a so-called Dopa decarboxylase (such as benserazide or carbidopa). This prevents L-dopa from being converted to dopamine in the blood, even before it reaches the brain. The dopa decarboxylase inhibitor can not even cross the blood-brain barrier. In the brain, L-Dopa can therefore be easily converted into dopamine.
Every Parkinson’s patient responds differently to L-Dopa. Therefore, the dosage is determined individually: The therapy is started with a low dose and then gradually increased until the desired effect occurs.
Mostly L-dopa must be taken several times a day. This should always be at the same times. This prevents a fluctuating effect.
It is also important that L-dopa is taken at least one hour before or after a protein-rich meal. Protein-rich foods disturb the absorption of the active ingredient into the blood.
Side effects:Parkinson’s therapy with L-dopa is generally very well tolerated, especially at low doses. Especially at the beginning of the therapy, however nausea occur. This can be well but with the active ingredient domperidone relieve. On the other hand, other medicines for nausea such as metoclopramide should not be used: they also cross the blood-brain barrier and can neutralize the effects of L-dopa.
Other possible side effects of L-Dopa are anorexia, dizziness, increased driveand depression, Older people, in particular, sometimes respond to treatment with L-dopa hallucinations, confusion and compulsive behavior.The latter manifests itself, for example, as a gambling or buying addiction, as a constant urge for food or sex or as compulsive ordering of objects.
Also movement disorders (Dyskinesias) are possible side effects of L-dopa: The affected patients twitch involuntarily or do jerky movementsthey can not prevent. The longer a person is treated with L-Dopa, the more frequent and severe such movement disorders become.
Long-term treatment with L-dopa can also cause the effect of the drug to fluctuate (effect fluctuations): Sometimes Parkinson’s patients can not move at all (“OFF-phase”), then completely normal again (“ON-phase”).
In such cases, it can help that Change dosing scheme of L-Dopa, Or else the patient gets on retarded L-dopa preparation um: The sustained-release tablets release the active ingredient more slowly and over a longer period of time than “normal” (non-retarded) L-dopa preparations. The treatment then usually works more evenly.
In case of fluctuations in L-Dopa (ON-OFF phases) and / or movement disorders, the doctor may also give the patient a portable drug pumpGive: It directs the levodopa automatically via a thin probe directly into the duodenum, where it is absorbed into the blood (duodenal probe). The active substance is thus administered continuously to the patient. This makes it possible to achieve very uniform blood levels in the blood. This reduces the risk of fluctuations in activity and movement disorders. However, a duodenal probe also carries risks, for example for peritonitis. Therefore, it is used only in selected cases and by experienced doctors.
An alternative to pump therapy is deep brain stimulation (see below).
Dopamine agonists
In patients younger than 70 years, Parkinson’s therapy is usually started with so-called dopamine agonists. Only later does the switch to the more effective L-Dopa take place. Thus one delays the occurrence of movement disorders, as they are triggered by the prolonged use of L-Dopa.
Dopamine agonists are chemically similar to the messenger substance dopamine. They easily cross the blood-brain barrier and dock at the same binding sites (receptors) of nerve cells as dopamine. Therefore, they also have a similar effect.
Most dopamine agonists used in Parkinson’s therapy are taken orally (for example as a tablet). This applies for example to pramipexole, piribedil and ropinirole. Other agents are administered as an active ingredient patch (rotigotine) or as a syringe or infusion (apomorphine).
Side effects: Dopamine agonists are less well tolerated than L-dopa. They cause, for example, water retention in the tissue (edema), constipation, drowsiness, dizzinessand nausea, Just like L-Dopa, dopamine agonists can also be used in older people hallucinations, confusion and compulsive behavior trigger.
With prolonged use, dopamine agonists can also effect variations (Fluctuations with ON-OFF phases) trigger. But that happens much less often than with L-Dopa. The fluctuating effect can be compensated by the dosage of the dopamine agonists is adjusted or the patient of the tablets on a drug patch (with rotigotine).
There is another possibility for effect fluctuations: the patient receives in addition to the tablets Spraying with apomorphine into the subcutaneous fat tissue (subcutaneously). Apomorphine can quickly relieve Parkinson’s discomfort, which is annoying despite tablet intake. Possible side effects include nausea, vomiting, increased or newly occurring movement disorders (dyskinesia), dizziness, hallucinations etc.
If all these attempts can not compensate for the fluctuations in effect, the patient may receive a portable medication pump (Apomorphine pump). Over a thin tube and a fine needle, it delivers the active substance to the subcutaneous fatty tissue on the abdomen or thigh continuously (usually over 12 to 18 hours).
So far, comprehensive studies on this apomorphine pump therapy are still missing. Studies show that they can significantly shorten the daily OFF phases (in which the patient can hardly move). Movement disorders (dyskinesias) can also decrease with the apomorphine pump.
Possible side effects are mainly skin reactions at the injection site of the needle, which can sometimes be severe (painful redness, Kötchenbildung, death of tissue = necrosis, etc.). Some patients also complain of nausea, vomiting, circulatory problems and hallucinations.
MAO-B inhibitors
MAO-B inhibitors (such as selegiline) inhibit the enzyme monoamine oxidase B (MAO-B), which normally degrades dopamine. In this way, the level of dopamine in the brain of Parkinson’s patients can be increased.
MAO-B inhibitors are less effective than levodopa or dopamine agonists. As sole Parkinson’s therapy, they are therefore only suitable for mild symptoms (usually in the early stages of the disease). But they can be combined with other Parkinson’s drugs (like L-Dopa).
Side effects: MAO inhibitors are considered to be well tolerated. They have only mild and reversible side effects. These include sleep disorders, because the drugs increase the drive. Therefore, you should take MAO-B inhibitors earlier in the day. Then the sleep is not disturbed in the evening.
COMT inhibitors
COMT inhibitors (such as entacapone) are prescribed together with L-dopa. They too block an enzyme that breaks down dopamine (the so-called catechol O-methyl transferase = COMT). In this way, COMT inhibitors prolong the effects of dopamine.
The active ingredients are mainly prescribed to reduce fluctuations in effect (fluctuations) under the treatment with L-dopa. So they are drugs for advanced Parkinson’s stages.
Side effects: COMT inhibitors are usually well tolerated. Possible unwanted effects include diarrhea, nausea and vomiting.
anticholinergics
The so-called anticholinergics were the first drugs that were used for Parkinson’s therapy. Today, they are not prescribed as often.
Due to the dopamine deficiency in Parkinson’s other messenger substances – in relative terms – in excess. This applies, for example, to acetylcholine. This causes among other things, the typical tremor (tremor) in the patients. It can be relieved with anticholinergics because they inhibit the action of acetylcholine in the brain.
Side effects: Anticholinergics can have a variety of side effects. These include, for example, dry mouth, dry eyes, reduced (rarely aggravated) sweating, disorders of bladder emptying, constipation, palpitations, photosensitive eyes, thought disorders and confusion.
Especially older people often do not tolerate anticholinergics very well. Therefore, the drugs are prescribed to younger patients.
NMDA antagonists
Like acetylcholine, the messenger glutamate in Parkinson’s is present in a relative excess due to dopamine deficiency. By contrast, so-called NMDA antagonists (amantadine, budipin) help. They block certain docking sites of glutamate in the brain and thus reduce its effect.
NMDA antagonists are used in the early stages of primary Parkinson’s disease.
Side effects:Possible unwanted effects of amantadine include restlessness, nausea, loss of appetite, dry mouth, retinal bluish changes (livedo reticularis), and confusion and psychosis (especially in the elderly). Budipin can cause dangerous cardiac arrhythmias.
Deep Brain Stimulation (DBS)
Deep brain stimulation (THS) is a surgical procedure in the brain. It is sometimes performed in idiopathic Parkinson’s syndrome. The English name is “Deep Brain Stimulation” (DBS).
In deep brain stimulation, small electrodes are inserted into certain areas of the brain during surgery. They are intended to positively influence (either stimulate or inhibit) the pathogenic activity of the nerve cells. Thus, deep brain stimulation works much like a pacemaker. It is sometimes called “Brain pacemaker“(Even if this term is not quite correct).
Deep brain stimulation comes into consideration when:
- can not relieve fluctuations in activity (fluctuations) and involuntary movements (dyskinesia) with medication or
- the tremor (tremor) can not be removed by medication.
In addition, the patient must meet even more requirements. For example, he may not show early symptoms of dementia. His general physical condition must be good. In addition, the parkinsonian symp- toms (except the tremor) must respond to L-dopa.
Experience has shown that the procedure can effectively alleviate the symptoms of many patients and significantly improve their quality of life. The effect seems to be persistent in the long term. However, that does not mean that deep brain stimulation can cure Parkinson’s – the disease progresses even after the procedure.
By the way: Originally, deep brain stimulation was performed especially in advanced Parkinson’s. However, studies have shown that it is also well-suited for patients under the age of 60, for whom L-Dopa therapy has only recently shown fluctuations in activity and causes movement disorders.
How does the procedure work?
Deep brain stimulation is performed in specialized clinics (THS centers). Before the operation, a sturdy metal frame is firmly fixed to the patient’s head. During the actual operation, the frame is firmly connected to the operating table. This keeps the head exactly in the same position all the time. This is necessary to be able to work with the medical instruments as precisely as possible (“stereotactic brain operation”).
Now, a computed tomography (CT) or magnetic resonance imaging (MRI) of the clamped in the frame head is made. Mit dem Computer lässt sich genau errechnen, in welchem Winkel und in welcher Tiefe im Gehirn die Elektroden eingesetzt werden müssen, damit dann die Elektrodenspitzen am richtigen Ort liegen. Der “richtige Ort” ist in der Regel ein winziges Areal im Gehirn, der sogenannte Nucleus subthalamicus (NST).
Als Nächstes folgt die eigentliche Operation: Der Neurochirurg bohrt mit einem speziellen Bohrer zwei kleine Löcher in die Schädeldecke, um darüber die winzigen Elektroden einzuführen. Das klingt brachial, ist aber für den Patienten nicht mit Schmerzen verbunden. Er ist während der gesamten Operation wach. Das ist nötig, damit der Chirurg die richtige Platzierung der Elektroden in einem Test überprüfen kann.
Am nächsten Tag wird unter Vollnarkose der Impulsgeber unter die Haut am Schlüsselbein oder am Oberbauch implantiert. Über kleine Kabel wird er mit den Elektroden im Gehirn verbunden. Die Kabel verlaufen unter der Haut.
Der Impulsgeber gibt kontinuierlich Strom an die Elektroden ab. Je nach Stromfrequenz werden dadurch die Areale an den Enden der Elektroden stimuliert oder gehemmt. So lindert sofort die motorischen Hauptsymptome der Parkinson-Erkrankung, also verlangsamte Bewegung, Muskelsteifheit und Zittern. Bei Bedarf lässt sich die Stromfrequenz mit einer Fernbedienung nachjustieren.
Sollte der Eingriff nicht den erwünschten Effekt haben, können die Elektroden wieder entfernt oder der Impulsgeber abgeschaltet werden.
Mögliche Komplikationen und Nebenwirkungen
Generell gilt: Die Tiefe Hirnstimulation scheint bei Patienten vor dem 50. Lebensjahr erfolgreicher zu sein und seltener Komplikationen zu verursachen als bei älteren Menschen.
Die wichtigste Komplikation, die sich durch die Hirnoperation selbst ergeben kann, sind Blutungen im Schädel (intrakranielle Blutungen). Außerdem kann das Einsetzen des Impulsgebers und der Kabel eine infection trigger. Dann muss meist das System vorübergehend herausgenommen und der Patient mit Antibiotika behandelt werden.
Bei fast jedem Patienten kommt es nach dem Eingriff, wenn das System noch eingestellt wird, zu vorübergehenden Nebenwirkungen. Das können zum Beispiel paresthesia (Parästhesien) sein. Diese treten aber oft nur direkt nach dem Einschalten des Impulsgebers auf und verschwinden dann wieder.
Weitere meist vorübergehende Effekte sind zum Beispiel Verwirrtheit, gesteigerter Antrieb, abgeflachte Stimmungand indifference (Apathie). Manchmal treten auch sogenannte Impulskontrollstörungen on. Dazu zählt zum Beispiel ein gesteigertes sexuelles Verlangen (Hypersexualität). Bei einigen Patienten löst die Tiefe Hirnstimulation auch leichte Sprechstörungen, one Störung der Bewegungskoordination (Ataxie), dizziness such as Gang- und Standunsicherheitout.
Weitere Therapiemethoden
Verschiedene Behandlungskonzepte können Parkinson-Patienten zusätzlich helfen, dass sie möglichst lange ihre Beweglichkeit, Sprechfähigkeit und Selbstständigkeit im Alltag bewahren. Die wichtigsten Verfahren sind:
Physiotherapie: Die Physiotherapie umfasst viele verschiedene Techniken. Die Patienten können zum Beispiel mit geeigneten Übungen ihr Gleichgewicht und ihre Sicherheit beim Gehen trainieren. Sinnvoll sind auch Kraft- und Dehnungsübungen. Die Schnelligkeit und der Rhythmus der Bewegungen lassen sich ebenfalls gezielt trainieren.
Logopädie: Viele Patienten entwickeln im Laufe der Parkinsonerkrankung eine Sprechstörung. Sie sprechen zum Beispiel auffallend monoton und sehr leise oder erleben wiederholt Blockaden beim Sprechen. Eine logopädische Therapie kann hier helfen.
Ergotherapie:Die Ergotherapie hat zum Ziel, dass die Parkinsonpatienten in ihrer persönlichen Umwelt möglichst lange selbstständig bleiben. Dafür passt man zum Beispiel den Wohnraum so an, dass der Patient sich besser zurechtfindet. Außerdem werden Stolperfallen wie Teppiche entfernt. Der Ergotherapeut entwickelt zusammen mit den Betroffenen auch Strategien, wie sich der Alltag mit der Erkrankung besser bewältigen lässt. So zeigt er den Patienten zum Beispiel den Umgang mit Hilfsmitteln wie Strumpfanzieher oder Knöpfhilfe. Zusätzlich berät der Therapeut die Angehörigen, wie sie den Parkinson-Patienten im Alltag sinnvoll unterstützen können.
Treatment of comorbidities
Das Parkinson-Syndrom betrifft oft ältere Menschen. Diese leiden meist zusätzlich noch an anderen Erkrankungen wie Bluthochdruck, Herzschwäche (Herzinsuffizienz), erhöhten Blutfettwerten oder Diabetes. Diese Begleiterkrankungen müssen ebenfalls fachgerecht behandelt werden. Das wirkt sich positiv auf die Lebensqualität und Lebenserwartung der Patienten aus.
Parkinson-Therapie: Was können Sie selbst tun?
Wie bei den meisten chronischen Beschwerden und Erkrankungen gilt auch für Parkinson: Betroffene sollten sich aktiv mit ihrer Erkrankung auseinandersetzen und sich über Ursachen und Behandlungsmöglichkeiten informieren. Denn in vielen Fällen ist es die Angst vor dem Ungewissen, welche die Patienten besonders belastet. Je mehr man über die Erkrankung erfährt, desto eher verschwindet das Gefühl der Machtlosigkeit gegenüber dem fortschreitenden Parkinson.
Heilbar ist die Erkrankung derzeit leider nicht. Mit der richtigen Behandlung ist für viele Patienten aber ein weitgehend normales Leben möglich.
Was Sie selbst zu einer wirksamen Therapie beitragen können, lesen Sie hier:
» Gehen Sie offen mit Ihrer Erkrankung um. Vielen Menschen mit Parkinson fällt es zunächst sehr schwer, die Erkrankung zu akzeptieren und offen damit umzugehen. Stattdessen versuchen sie, die Symptome zu verstecken. So setzt man sich selbst aber unter unnötigen Druck. Wenn Sie offen mit Freunden, Angehörigen und Arbeitskollegen über Ihre Erkrankung sprechen, wird Ihnen das eine gewaltige Last von den Schultern nehmen.
» Informieren Sie sich über die Krankheit. Je mehr Sie über Parkinson wissen, desto weniger unheimlich erscheint er Ihnen vielleicht. Auch als Angehöriger eines Parkinson-Patienten sollten sie sich über die Erkrankung informieren. So können Sie Ihren Angehörigen wirksam und sinnvoll unterstützen.
» Schließen Sie sich einer Parkinson-Selbsthilfegruppe an. Wer sich regelmäßig mit anderen Betroffenen austauschen kann, kommt oft besser mit der Erkrankung zurecht.
» Bleiben Sie fit. Sie können einen guten Allgemeinzustand bewahren, werden Sie körperlich aktiv bleiben. Dazu genügen schon regelmäßige Bewegung (wie Spaziergänge) und leichter Ausdauersport. Die Angehörigen können den Patienten dabei unterstützen.
» Kleine Hilfen im Alltag. Viele Parkinson-Symptome erschweren des Alltag. Dazu zählt etwa das sogenannte “Einfrieren” (Freezing) – der Betreffende kann sich dabei nicht mehr bewegen. Hier helfen visuelle Reize auf dem Boden, beispielsweise aufgeklebte Fußabdrücke, oder akustische Rhythmusgeber (“Links, zwo, drei, vier”). Wichtig für Mitmenschen: Es macht keinen Sinn, den Patienten zur Eile zu drängen oder zu ziehen. Dies verlängert die “Einfrier”-Episode eher.
» Gesunde Ernährung. Menschen mit Parkinson essen und trinken oft zu wenig, weil sie ungeschickt und langsam sind. Manche möchten auch den anstrengenden Toilettengang möglichst vermeiden. Für einen gesunden Allgemeinzustand ist es aber sehr wichtig, dass man ausreichend Flüssigkeit (etwa zwei Liter am Tag) zu sich nimmt und sich ausgewogen ernährt.
Parkinson: Fachkliniken
Menschen mit dem Parkinson-Syndrom sollten nach Möglichkeit in einer Fachklinik behandelt werden. Ärzte und sonstige Mitarbeiter dort sind auf die Erkrankung spezialisiert.
Mittlerweile gibt es in Deutschland zahlreiche Kliniken, die eine Akutbehandlung und/oder Rehabilitation für Parkinson-Patienten anbieten. Einige davon tragen ein Zertifikat der Deutsche Parkinson Vereinigung (dPV). Es wird an Krankenhäuser und Rehabilitationseinrichtungen verliehen, die spezielle diagnostische und therapeutische Angebote für Menschen mit Parkinson und verwandte Erkrankungen haben. Das Zertifikat der dPV wird den Spezial-Kliniken für drei Jahre verliehen. Auf Wunsch der jeweiligen Einrichtung kann es nach erneuter Prüfung jeweils für weitere drei Jahre verlängert werden.
Eine ausgewählte Liste von Spezialkliniken für Parkinson-Patienten finden Sie im Beitrag Parkinson – Klinik.
Parkinson: Untersuchungen und Diagnose
Wenn Sie den Verdacht einer Parkinson-Erkrankung bei sich selbst oder einem Angehörigen haben, ist der Besuch bei einem fachkundign Arzt ratsam. Der Spezialist für Erkrankungen des Nervensystems ist der Neurologe, Am besten gehen Sie zu einem Neurologen, der auf die Diagnose und Behandlung von Parkinson spezialisiert ist. An manchen neurologischen Kliniken gibt es auch eigene Sprechstunden beziehungsweise Ambulanzen für Parkinson-Patienten.
Doctor-patient conversation
Beim ersten Besuch wird der Neurologe im Gespräch mit Ihnen beziehungsweise dem betroffenen Angehörigen die Krankengeschichte erheben (anamnese). Für die Parkinson-Diagnose ist dieses Gespräch enorm wichtig: Wenn der Patient seine Beschwerden ausführlich schildert, kann der Arzt einschätzen, ob es sich tatsächlich um Parkinson handeln könnte. Mögliche Fragen des Arztes sind zum Beispiel:
- Seit wann ungefähr besteht das Zittern (Tremor) der Hände/Beine?
- Haben Sie das Gefühl, dass Ihre Muskulatur ständig angespannt ist?
- Haben Sie Schmerzen, etwa im Schulter- oder Nackenbereich?
- Fällt es Ihnen schwer, beim Gehen das Gleichgewicht zu halten?
- Fallen Ihnen feinmotorische Tätigkeiten (zum Beispiel ein Hemd zuknöpfen, Schreiben) zunehmend schwer?
- Haben Sie Probleme beim Schlafen?
- Ist Ihnen aufgefallen, dass sich Ihr Geruchssinn verschlechtert hat?
- Wurde bereits bei Angehörigen eine Parkinson-Erkrankung festgestellt?
- Nehmen Sie Medikamente ein, beispielsweise aufgrund psychischer Probleme? (Antipsychotika, „Dopaminantagonisten“ wie Metoclopramid)
Körperliche und neurologische Untersuchung
Neben dem Anamnesegespräch folgen eine körperliche und eine neurologische Untersuchung. Dabei überprüft der Arzt allgemein die Funktion des Nervensystems: Er testet zum Beispiel die Reflexe des Patienten, die Empfindsamkeit (Sensibilität) der Haut und die Beweglichkeit der Muskeln und Gelenke. Dabei achtet er besonders auf die Hauptsymptome von Parkinson:
Verlangsamte Bewegungen (Bradykinese) sind sehr charakteristisch für Parkinson. Der Arzt erkennt sie, indem er Ihren Gang, Ihre Gestik und Mimik beobachtet. Möglicherweise wird er Sie bitten, einige Meter im Untersuchungsraum entlang zu gehen. Dabei kann er auch beurteilen, ob Sie „wackelig auf den Beinen“ sind (posturale Instabilität).
Um festzustellen, ob Ihre Muskeln auffallend steif sind (Rigor), wird der Arzt prüfen, ob sich Ihre Gelenke flüssig bewegen lassen. Bei Parkinson ist die Muskelspannung stark erhöht, so dass die Muskeln einen Widerstand entgegensetzen, wenn der Arzt versucht, ein Gelenk (wie den Ellenbogen) zu bewegen. Dieses Phänomen wird auch als Zahnradphänomen bezeichnet (siehe oben: “Parkinson: Symptome”).
Ob bei Ihnen ein Zittern in Ruhe (Ruhetremor) vorliegt, bemerkt der Arzt während der körperlichen Untersuchung. Wichtig für die Parkinson-Diagnose ist die Unterscheidung zwischen einem Ruhetremor (wie er bei Parkinson auftritt) und anderen Tremorarten. Dazu zählt zum Beispiel der sogenannte Intentionstremor: Bei einer Schädigung im Kleinhirn beginnt die Hand zu zittern, sobald der Betreffende versucht, eine gezielte Bewegung damit auszuführen. In Ruhe zittert die Hand dagegen nicht.
Parkinson-Test (L-Dopa-Test)
Um die Parkinson-Diagnose zu unterstützen, wird manchmal der sogenannte L-Dopa-Test durchgeführt. Dabei erhalten Patienten einmalig die Dopamin-Vorstufe L-Dopa (Levodopa). Das ist jenes Medikament, das zur Standardtherapie bei Parkinson gehört. Bei manchen Patienten bessern sich die Bewegungsstörungen und die steifen Muskeln schon kurz nach der Einnahme (ungefähr eine halbe Stunde danach). Dann liegt vermutlich ein idiopathisches Parkinson-Syndrom vor (Achtung: Der Ruhe-Tremor lässt sich nicht immer mit Levodopa lindern).
Der L-Dopa-Test ist in der Parkinson-Diagnostik aber nur begrenzt aussagekräftig. Denn manche Menschen haben zwar Parkinson, sprechen aber nicht auf den Test an. Dann fällt das Ergebnis falsch-negativ aus. Umgekehrt kann der L-Dopa-Test auch bei anderen Erkrankungen als Parkinson positiv ausfallen. Das gilt zum Beispiel bei manchen (aber nicht allen) Patienten mit einer sogenannten Multisystematrophie. Bei dieser fortschreitenden Erkrankung sterben Nervenzellen in verschiedenen Hirnregionen ab. Das kann ein atypisches Parkinson-Syndrom auslösen.
Wegen dieser Probleme wird der L-Dopa-Test nicht routinemäßig in der Parkinson-Diagnostik empfohlen. Ein weiterer Grund dafür ist, dass er Nebenwirkungen wie Übelkeit und Erbrechen haben kann. Um diesen vorzubeugen, erhalten Patienten vor dem Test in der Regel das Anti-Brechmittel Domperidon.
Der L-Dopa-Test kann auch helfen, die Therapie bei Parkinson zu planen: Bei nachgewiesenem Parkinson kann mit dem Test geprüft werden, wie gut der Patient auf L-Dopa anspricht. Aber auch hier darf man kein eindeutiges Testergebnis erwarten. Manche Patienten sprechen nicht auf den Test an (negatives Ergebnis), lassen sich später aber trotzdem gut mit L-Dopa behandeln.
By the way: Anstelle des L-Dopa-Tests wird zur Parkinson-Diagnose gelegentlich der Apomorphin-Test gemacht. Hier wird geprüft, ob sich die Bewegungsstörungen nach einer Apomorphin-Spritze bessern. Wenn ja, spricht dies für ein idiopathisches Parkinon-Syndrom. Es gilt hier aber das Gleiche wie beim L-Dopa-Test: Nicht bei jedem Parkinson-Patient fällt der Test positiv aus. Zudem können Nebenwirkungen wie Übelkeit, Erbrechen oder Schläfrigkeit auftreten.
Imaging procedures
With the help of Computed tomography (CT) oder der Magnetic Resonance Imaging (MRI) lässt sich das Gehirn des Patienten bildlich darstellen. Das kann helfen, andere mögliche Ursachen für die vermuteten Parkinson-Symptome auszuschließen, beispielsweise einen Hirntumor. Die Bildgebung des Gehirns hilft also, ein idiopathisches Parkinson-Syndrom von einem sekundären Parkinson oder anderen neurodegenerativen Erkrankungen (wie atypischer Parkinson) zu unterscheiden.
Eventuell werden dazu auch spezielle Untersuchungen durchgeführt. Dazu gehört beispielsweise die SPECT (Single Photon Emission Computed Tomography), eine nuklearmedizinische Untersuchung: Dem Patienten wird dabei zuerst eine radioaktive Substanz verabreicht. Mit dieser lassen sich jene Nervenenden im Gehirn darstellen, die sich bei Parkinson zurückbilden (DAT-SPECT). Das kann Aufschluss in unklaren Fällen geben.
Wenn die Parkinson-Diagnose unklar ist, ordnet der Arzt manchmal auch eine spezielle Variante der Positronen-Emissions-Tomografie (PET) an: die FDG-PET, Die Abkürzung FDG steht für Fluordesoxyglukose. Das ist ein radioaktiv markierter Einfachzucker. Er wird dem Patienten verabreicht, bevor man das Gehirn bildlich mittels PET darstellt. Diese Untersuchung kann vor allem helfen, ein atypisches Parkinson-Syndrom abzuklären. Allerdings ist die Untersuchung zu diesem Zwecke nicht offiziell zugelassen. Sie wird deshalb nur in begründeten Einzelfällen dazu eingesetzt (“off-label-use”).
Weniger aufwändig und kostengünstiger als diese Spezialuntersuchungen ist die Ultraschalluntersuchung des Gehirns (Transkranielle Sonografie, TCS). Sie hilft, ein idiopathisches Parkinson-Syndrom im Frühstadium zu erkennen und gegen andere Erkrankungen (wie atypische Parkinson-Syndrome) abzugrenzen. Dazu sollte der Arzt mit dieser Untersuchung aber umfassende Erfahrungen besitzen. Anderenfalls kann er das Untersuchungsergebnis vielleicht nicht richtig interpretieren.
Wie wird letztlich die Parkinson-Diagnose gestellt?
Es ist nach wie vor oft schwer, die Diagnose Parkinson zweifelsfrei zu stellen. Ein Grund dafür ist, dass es viele verschiedene Erkrankungen gibt, die ähnliche Symptome wie die Parkinson-Erkrankung auslösen.
Das Arzt-Patient-Gespräch (Anamnesegespräch) und die körperlich-neurologische Untersuchung sind essenziell für die Parkinson-Diagnostik. Die weiteren Untersuchungen dienen in erster Linie dazu, andere Gründe für die Symptome auszuschließen. Nur wenn sich die Beschwerden gut durch Parkinson erklären lassen und keine anderen Ursachen dafür gefunden werden, kann die Parkinson-Diagnose (Idiopathisches Parkinson-Syndrom) gestellt werden.
Sonderfall: Genetisch bedingter Parkinson
Wie im Abschnitt “Ursachen” erwähnt, sind genetisch bedingte Formen von Parkinson sehr selten. Sie lassen sich aber mit einer molekulargenetischen Untersuchung determine. Eine solche Untersuchung kommt in Betracht, wenn:
- der Patient vor dem 45. Lebensjahr an Parkinson erkrankt oder
- mindestens zwei Verwandte 1. Grades an Parkinson leiden.
In diesen Fällen liegt der Verdacht nahe, dass die Parkinson-Erkrankung durch eine Genmutation verursacht wird.
Gesunde Angehörige eines Patienten mit genetisch bedingtem Parkinson können sich ebenfalls einem Gentest unterziehen. So lässt sich feststellen, ob auch sie die auslösende Genmutation aufweisen. Ein solcher Gentest zur Abschätzung des persönlichen Parkinson-Risikos darf aber erst durchgeführt werden, nachdem der Betreffene von einem Facharzt ausführlich genetisch beraten wurde.
Disease course and prognosis
Das idiopathische Parkinson-Syndrom ist eine fortschreitende Erkrankung, die bislang nicht heilbar ist. Je nach Symptomatik unterscheiden Mediziner vier Verlaufsformen:
- akinetisch-rigider Typ: Es treten vor allem Bewegungslosigkeit und Muskelsteife auf, während Tremor kaum oder gar nicht vorhanden ist.
- Tremordominanz-Typ: Das Hauptsymptom ist das Zittern (Tremor).
- Äquivalenz-Typ: Bewegungslosigkeit, Muskelsteife und Zittern sind ungefähr gleich ausgeprägt.
- monosymptomatischer Ruhe-Tremor: Das Zittern in Ruhe ist das einzige Symptom. Sehr seltene Verlaufsform.
Neben der Verlaufsform spielt das Erkrankungsalter eine wichtige Rolle bei Parkinson: Verlauf und Prognose werden davon beeinflusst, ob die Erkrankung in verhältnismäßig jungem Lebensalter (beispielsweise ab dem 40. Lebensjahr) oder aber im höheren Alter ausbricht.
So passiert es bei jüngeren Patienten viel eher, dass die Parkinson-Medikamente Bewegungsstörungen (Dyskinesien) und Wirkungsschwankungen (Fluktuationen) auslösen. Das trifft besonders beim akinetisch-rigiden Parkinson-Typ zu, für den ein frühes Erkrankungsalter typisch ist. Dafür ist L-Dopa bei diesen Patienten gut wirksam.
Anders beim Tremordominanz-Typ: Die Betroffenen sprechen relativ schlecht auf L-Dopa an. Dafür schreitet bei ihnen der Parkinson langsamer voran als bei den anderen Verlaufsformen. Somit hat der Tremordominaz-Typ die günstigste Prognose.
Parkinson: Lebenserwartung
Mitte der 1970er Jahre wurden moderne Parkinson-Medikamente wie Levodopa entwickelt. Das veränderte die Prognose bei “echtem” (idiopathischem) Parkinson: Lebenserwartung und Lebensqualität der Patienten verbesserten sich dank der neuen Wirkstoffe. Laut Statistik hat ein optimal behandelter Parkinson-Patient heute fast die gleiche Lebenserwartung wie eine gleichaltrige gesunde Person: Wenn heute jemand mit 63 Jahren die Diagnose Parkinson bekommt, kann er schätzungsweise noch mit weiteren 20 Lebensjahren rechnen. Zum Vergleich: Mitte des letzten Jahrhunderts lebten Patienten nach der Diagnose im Schnitt noch etwas mehr als neun Jahre.
Die gestiegene Lebenserwartung beim idiopathischen Parkinson-Syndrom kommt dadurch zustande, dass die modernen Medikamente die wesentlichen Beschwerden der Patienten weitgehend beheben. Früher führten solche Beschwerden oft zu Komplikationen, die dann den Patienten vorzeitig sterben ließen. Ein Beispiel: Parkinson-Patienten, die sich kaum noch bewegen konnten (Akinesie), waren oft bettlägerig. Diese Bettlägerigkeit lässt das Risiko für gefährliche Erkrankungen wie Thrombose oder Lungenentzündung massiv ansteigen.
Die verbesserte Lebenserwartung, wie sie hier beschrieben ist, bezieht sich nur auf das idiopathische Parkinson-Syndrom (= den „klassischen Parkinson“). Atypische Parkinson-Syndrome, bei denen die Betroffenen nicht oder kaum auf eine Behandlung mit L-Dopa ansprechen, schreiten meist rascher voran. Sie haben in der Regel eine deutlich schlechtere Prognose.
Additional information
Book recommendations:
- Parkinson – das Übungsbuch: Aktiv bleiben mit Bewegungs-Übungen (Elmar Trutt, 2017, TRIAS)
- Parkinson: Ein Ratgeber für Betroffene und Angehörige (Willibald Gerschlager, 2017, Facultas / Maudrich)
guidelines:
- S3-Leitlinie “Idiopathisches Parkinson-Syndrom” der Deutschen Gesellschaft für Neurologie (Stand: 2016)
Support Groups:
Deutsche Parkinson Vereinigung e.V.:
https://www.parkinson-vereinigung.de